Лечение блд в домашних условиях

Организм новорожденного сильно уязвим, особенно у недоношенных. Органы и системы детей, появившихся раньше срока, отличаются морфологической незрелостью. При нарушении функции дыхания и газообмена прибегают к искусственной вентиляции легких (ИВЛ).
Вследствие некомпетентности, неорганизованности медицинских работников во время выполнения ИВЛ у грудничков развивается бронхолегочная дисплазия (БДЛ). Общий показатель смертности при повреждении тканей нижних дыхательных путей – 10-25%. У выживших сохраняются морфологические изменения альвеол.
Что такое бронхолегочная дисплазия
В ранний постнатальный период в организме преждевременно рожденных плохо развита реакция на раздражители. Взаимодействие между разными системами не налажено. Пневмотаксический центр, находящийся в головном мозге и обеспечивающий правильное чередование вдоха и выдоха, сформирован не до конца. Дыхание неравномерное, прерывается респираторными паузами. Детям, недавно появившимся на свет, с массой тела ниже 1500 г, нередко требуется кислородная терапия. При неправильном расчете концентрации кислорода во время проведении аппаратной вентиляции возникает бронхолегочная дисплазия.
После постановки диагноза оповещают мать маленького пациента. Чтобы понять, что угрожает ребенку, следует разобраться, что такое бронхолегочная дисплазия. Патология относится к поздним патологическим изменениям, развивающимся у детей в результате длительной нерациональной аппаратной вентиляции легких.
Патология относится к ятрогенным – развивается вследствие безалаберности медсестер, докторов при выполнении ИВЛ. Недоношенные дети нуждаются в специальном уходе. Малышам с проблемами дыхания проводят аппаратную вентиляцию с высокими концентрациями кислорода.
Для новорожденных применяется метод ИВЛ с ограничением давления: вдох заканчивается в момент, когда давление достигает заданного максимального параметра. Поток распределяется относительно равномерно, а метод считается более безопасным.
Аппаратная вентиляция легких требует пристального наблюдения за состоянием маленького пациента и точного расчета кислорода и давления. Следует учитывать растяжимость легких. Установка подбирается индивидуально, врач не менее часа находится у юовеза, следит за дыханием, оптимизируя вентиляцию.
В условиях обычных стационаров расчет давления проходит по одной формуле без учета индивидуальных особенностей. В результате избыток кислорода приводит к деструкции.
Почему возникает у недоношенных детей
Анатомически легкие состоят из бронхов, заканчивающихся бронхиолами с альвеолами на концах. Последние представляют собой воздушные пузырьки, покрытые множеством кровеносных сосудов. При вдохе пузырьки расширяются, при выдохе – уменьшаются, а находящийся внутри кислород переходит в кровь, CO₂ удаляется обратно. Альвеолы покрыты сурфактантом, не дающим пузырькам слипаться и меняющим их натяжение в зависимости от того, вдох это или выдох.
Сурфактант вырабатывается начиная с 26 недели беременности. Дети, рожденные в период с 28 по 38 неделю гестационного периода, испытывают недостаток поверхностного вещества и проблемы с дыханием. Для восстановления легочной функции пациентам назначают медикаментозную и кислородную терапию.
Недоношенные дети, родившиеся в гестационным возрасте от 23 до 30 недель – во время канальцевой и саккулярной стадии развития легкого, подвергаются наибольшему риску возникновения БЛД.
На развитие бронхолегочной дисплазии у недоношенных детей влияет ряд факторов:
1. Механическая травма. Незрелые легкие трудно проветривать из-за дефицита сурфактанта. При недостатке поверхностного вещества ухудшается растяжимость дыхательных органов, развиваются проблемы с функциональной остаточной способностью. При вентиляции легкие расширяются неравномерно с очаговыми перенапряжениями и ателектазом (спадения доли). Положительное давление и избыточный объем при проведении вентиляции приводят к чрезмерному надуванию легкого, повреждению клеток, воспалению.
2. Кислородная токсичность. Супрафизиологический кислород приводит к увеличению генерации митохондриальных активных форм О₂. Вследствие дефицита антиоксидантов и незрелой защиты повышается восприимчивость к окислительному стрессу и повреждению альвеолярных клеток в развивающемся легком.
3. Инфекция и воспаление. Кроме всего прочего, у преждевременно родившегося ребенка не сформирован иммунитет. Постнатальные воспаления, внутрибольничная инфекция ухудшают функции дыхательного органа. Часто у малышей, получавших в первую неделю жизни курсы антибиотиков, развивается резистентность грамотрицательных бактерий. В результате сложно подобрать медикамент и развивается более тяжелая инфекция, поражающая ткани органов дыхания.
4. Генетика. У малышей, преждевременно появившихся на свет, гены антиоксидантов (каталаза, SOD, глутатионпероксидаза), обеспечивающие защиту против активных форм кислорода, обладают низкой активностью. Кислород активизирует другие гены, ответственные за синтез противовоспалительных цитокинов, что приводит к увелечению нейрофилов.
У недоношенных новорожденных легкие часто подвергаются нескольким источникам травм как до, так и после рождения. Эти воздействия, наряду с генетической предрасположенностью к патологиям легких, могут вызвать прямое повреждение паренхимы дыхательных органов с последующим отклонением от нормального пути развития.
Классификация
В неонатологии уделяют две основные формы БЛД:
1. Классическая («тяжелая») – развивается у новорожденных, к которым применялись жесткие режимы аппаратной вентиляции, без заменительной сурфактатной терапии.
2. Новая (постсурфактантная) – возникает у детей гестационного возраста 28-32 недели, которым вводился сурфактант.
В отечественной неонатологии классификация бронхолегочной дисплазии определяется степенью тяжести патологии:
· легкая – дыхание комнатное до 56 дня постнатального возраста;
· умеренная – приступы тахиапноэ, при плаче, кормлении. Необходима распираторная поддержка;
· тяжелая – требуется проведение вентиляции с положительным давлением и концентрацией кислорода >30%.
Классическая форма
Представляет собой тяжелую хроническую форму заболевания легких, возникающее после респираторно-депрессивного синдрома до введения сурфактанта. Данная форма бронхолегочная дисплазия наблюдается у детей любого гестационного возраста. Патогенетические факторы: респираторная недостаточность, требующая ИВЛ, неонатальная пневмония, гипоплазия легких, синдром аспирации мекония.
Форма чаще встречается у мальчиков и обратно пропорционально связана с тем, сколько было недель при рождении и каков был вес. Патология характеризуется повышенным сопротивлением дыхательных путей при воспалении и гиперчувствительностью бронхов. Течение часто осложняется патологиями инфекционного генезиса с последующим развитием нарушения газообмена в органах дыхательной системы и крови.
Патологические признаки классической формы:
· чередование ателектаза с гиперинфляцией легких;
· тяжелые эпителиальные поражения дыхательных путей: антенотальное недоразвитие, сквамозные изменения эпителия;
· выраженная недоразвитость структурных элементов гладких мышц легких;
· обширная, диффузная фибропролиферация;
· гипертрофирование легочных артерий;
· снижение альвеоляризации и площади поверхности.
По статистике при тяжелой форме БЛД выживаемость составляет 71-81%.
Новая форма
Чаще всего возникает у малышей, рожденных на 24-28 неделях гестационного периода, с массой тела от 400 г до одного килограмма. Основные факторы, влияющие на развитие: морфологическая незрелость легких, нарушение развития паренхимы, «воздушных пузырьков» и сосудов легочного ствола.
Дети с новой формой бронхолегочной дисплазии в первые несколько суток жизни испытывают незначительную потребность в О₂. И только спустя несколько недель функции легких ухудшаются, характеризуется нарушениями газообмена.
Патологические признаки новой формы:
· менее регионарная гетерогенность заболеваний легких;
· редкие эпителиальные поражения органов дыхания;
· мягкое утолщение гладких мышц легких;
· небольшие изменения фибропролиферации;
· наличие небольшого числа «дисморфных» артерий.
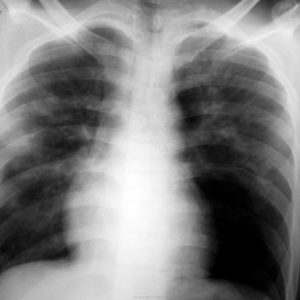
При ухудшении на рентгенографии наблюдается «туманность» легких, что свидетельствует о повышении альвеолярно-капиллярной проницаемости.
Симптомы у новорожденных
БЛД не отличается специфической клинической картиной. Первые проявления такие же, как и при респираторном дистресс синдроме (РДС). Симптомы бронхолегочная дисплазия у новорожденных:
· нарушение нормального газообмена, обусловленное высокими дозами кислорода, подаваемого длительное время во время аппаратной вентиляции;
· медиастинальная эмфизема;
· скопление газа в плевральной полости, которое ведет к спадению легкого;
· приступы апноэ;
· аритмия с ЧСС менее 60 уд./мин.
Из визуальных признаков – грудная клетка увеличивается в размерах, похожа на бочку.
Клинические рекомендации по защите легких от повреждения
Поскольку патогенез заболевания многофакторный применяются разнообразные подходы, направленные на защиту от повреждений легких и развития БЛД.
При терапии бронхолегочной дисплазия у детей придерживаются клинических рекомендаций, которые доказали свою эффективность.
1. Стратегия проведения ИВЛ. Для снижения вероятности травматизации дыхательных органов проводится «мягкая вентиляция» – минимальная либерализация мишеней СО₂ (>52 против <48 мм рт. ст). Эффективно использование неинвазивных методов вентиляции с положительным давлением, двухуровневой назальной и носовой канюлей с высоким расходом.
2. Экзогенный сурфактант. Заменительная терапия с применением активного поверхностного вещества животного происхождения снижает частоту скопления воздуха в плевральной полости, улучшает оксигенацию.
3. Применение кортикостероидов. Глюкокортикоиды снижают частоту развития патологии за счет уменьшения воспаления, а также индукции изменения созревания легких. Для уменьшения негативного воздействия гормональных препаратов на неокрепшую нервную систему применяют эндотрахеальный будесонид с сурфактантом.
4. Кофеин. Использование вещества позволяет снизить продолжительность аппаратной вентиляции. Вещество широко используется при терапии апноэ. Единственный побочный эффект – снижение весовых прибавок.
5. Витамин А. Ретинол играет важную роль в поддержании целостности эпителия дыхательных путей и является ключевым регулятором нормального роста легких. Препарат вводится внутримышечно, что связано с дискомфортом и повышенным риском инфицирования.
Последствия и прогноз жизни
Давать долгосрочные прогнозы трудно, поскольку нужно учитывать, что раннее применялось устаревшее лечение. Воздействие на позднее состояние здоровья легких и последствия дополнительного инфекционного поражения охарактеризованы плохо.
Исследования детей, переживших БЛД показывают, что наблюдаются нарушения общих и защитные функций легких, астматоподобне симптомы, легочная гипертония, склонность к гипоксии.
Последствия бронхолегочной дисплазии у недоношенных детей можно резюмировать следующим:
1. Нарушение функций легких. У выживших уменьшается процент объема форсированного выдоха за 1 секунду. У некоторых пациентов с возрастом функции органа дыхания ухудшаются. Это связано с дисанаптическим ростом, при котором дыхательные пути растут менее быстро, чем паренхима легкого, что приводит к фиксированной непроходимости путей.
2. Нарушение защитных функций. Респираторные инфекции у перенесших БЛД вызывают более тяжелые заболевания. Повышенная склонность к патологиям дыхательной системы вызывает дополнительные повреждения в и без того уязвимом легком. Помимо внешнего негативного воздействия, патологический процесс осложняется хроническим рефлюксом и микроаспирацией с риском аспирационной пневмонии.
3. Астмаподобные симптомы. Исследования показали, что у 25% детей, родившихся <26 недель, в возрасте 10-11 лет диагностируется астма. При подозрении на астму и назначении бронходилататоров реакция на данные препараты снижена из-за сужения периферических дыхательных путей.
4. Нарушение газообмена. Из-за нарушения хеморецепторной функции, изменения содержания кислорода приводят к аномальным дыхательным реакциям — гипоксии, гипероксии. Также увеличивается риск нарушения функций дыхательных мышц.
5. Легочная артериальная гипертензия (ЛГ). Дисморфная легочная сосудистая сеть и нарушенный онтогенез приводят к риску повышения легочного давления. У детей с ЛГ высок риск развития поздних заболеваний сосудистой системы дыхательных органов. Применяемая стандартная вазодилататорная терапия может привести к дополнительному ингибированию пролиферации гладкомышечных клеток.
В течение первого года жизни 49% детей с БЛД требуется повторная госпитализация, и риски смертности, связанные с осложнениями, значительны.
Заключение
Определение, патофизиология, терапия бронхолегочной дисплазии значительно изменились с момента первого описания патологии. Междисциплинарная помощь, направленная на решение сложных легочных проблем, потребностей в питании и развитии имеет решающее значение и может влиять на исходы тяжелой формы БЛД.
Рендомизированные терапевтические исследования в дополнение к продольной оценке пациентов остаются необходимыми для оптимизации медицинской помощи и для дальнейшего выявления факторов риска. Тенденция демонстрирует увеличение выживаемости детей рожденных <26 недель. У половины из них диагностируется БЛД, поэтому крайне важно, чтобы в будущих исследованиях максимально были изучены механизмы и факторы, влияющие на развитие легочных постсиндромов, с целью снижения бремени болезней.
Если Вам понравилась статья пожалуйста поставьте Лайк и подпишитесь на канал, чтобы не пропустить новый материал!
Информация, размещенная на канале Дзен, носит ознакомительный характер. Обязательно проконсультируйтесь со специалистом.
Источник
БЛД, или бронхолегочная дисплазия – хроническое заболевание, которое развивается у недоношенных детей в связи с проведением искусственной вентиляции легких. В результате у ребенка происходит повреждение слаборазвитых бронхов и легких кислородом высокой концентрации, что проявляется стойкими обструктивными нарушениями.
Возникает вопрос: Почему недоношенный ребенок не может дышать сам и его необходимо подключать к аппарату искусственного вентилирования легких (ИВЛ)?

Доктор Никонов
Мое мнение: акт дыхания безусловный и начинается с движения мышцы, которая называется диафрагмой, создающей в легких вакуум и туда, как в насос, под давлением поступает воздух. Объем поступающего воздуха зависит от того, могут ли межреберные мышцы растянуться полностью или нет.
У доношенных детей межреберные мышцы растягиваются полностью, альвеолы в легких полностью заполняются воздухом, слизь в них не скапливается.
У недоношенных детей межреберные мышцы полностью растянуться не могут, поэтому часть альвеол не заполняется воздухом.
Чтобы в этом убедиться, я посмотрел в электронный микроскоп на срез межреберной мышцы недоношенного ребенка, умершего от отека легких, возникшего от бронхолегочной дисплазии или БЛД.
В электронный микроскоп виден отек в межреберной мышце.

Пояснение к представленному выше фото:
- Красным цветом показаны мышечные волокна, которые находятся на расстоянии друг от друга. В норме мышечные волокна расположены параллельно и прижаты друг к другу.
- Желтым цветом на фото изображен отек, давящий на мышечные волокна, дезорганизуя их.
- Отодвигающий ядра клеток (темные точки) от центра к периферии и затрудняющий работу митохондрий, вырабатывающих энергию для растяжения мышц.
Чтобы ребенок не умер от удушья, его подключают к аппарату искусственного дыхания.
Лечение бронхолегочной дисплазии у новорожденных без лекарств
Вы можете задать вполне объективный вопрос: “Почему у меня получается избавить недоношенного ребенка от бронхолегочной дисплазии?”. Я врач-миолог и подхожу к лечению БЛД с точки зрения специалиста по мышцам. Когда у ребенка после моего воздействия на мышцы методом Никонова проходят хрипы, перестают возникать бронхиты и он начинает восстанавливаться, тогда становиться понятна правильность моих объяснений.
Посмотрите, как уменьшается отек в межреберных мышцах у детей с бронхолегочной дисплазией во время воздействия на мышцы методом Никонова:
- На первом фото отек очень сильный: ребенок не может самостоятельно дышать и находится на аппарате искусственной вентиляции легких (ИВЛ).

- На втором фото отек стал меньше в результате моей работы. В этом состоянии межреберные мышцы могут растягиваться длиннее. Альвеолы полностью заполняются воздухом, обструктивный бронхит больше не возникает. Апноэ у ребенка не наблюдается.
Это результат лечения новорожденного ребенка с бронхолегочной дисплазией воздействием на мышцы по методу Никонова с фиксацией проблемной мышцы.
- На третьем фото отек межреберных мышц еще больше уменьшился. Процедуры воздействия на мышцы методом Никонова продолжаются. У ребенка прекратились хрипы, дыхание стало чистым и ровным.
Причины возникновения отека в межреберных мышцах
В данной части статьи я расскажу о причинах возникновения отека межреберных мышц у недоношенных детей с точки зрения знаний 21 века.
Профессор Kiyotoshi Sekiguchi, университет Осаки, Япония:
Примитивная (до 9 недель развития эмбриона) лимфатическая система перестает расти и не ветвиться из-за того, что белок-строитель полидом не вырабатывается эндотелиальными клетками и клетками мезенхимы.
Мышечные клетки растут, а лимфатические сосуды не растут.

Доктор Никонов
Лимфа забирает отходы жизнедеятельности клеток и выводит их из организма ребенка. Но так как лимфатических сосудов становиться меньше по отношению к мышечным волокнам, то не все отходы выводятся лимфой. Так начинается отек в межреберных мышечных волокнах.
В незрелых легких недоношенных детей имеется дефицит сурфактанта – естественного поверхностного-активного вещества, которое препятствует слипанию альвеол на выдохе и необходимого для удаления слизи реснитчатым эпителием. Поверхностно-активное вещество начинает синтезироваться на 20-24 недели гестации, необходимый уровень сурфактанта достигается к 35-36 неделе.
Неврологи отмечают, что БЛД, т.е. бронхолегочная дисплазия, имеет ятрогении.
Искусственная вентиляция легких особенно в жестких режимах приводит к баротравме бронхиальной и легочной тканей, про этом токсическое действие высоких концентраций кислорода вдыхаемой смеси также приводит к повреждению эпителия, развитию отека легочной ткани и пропитыванию ее белком. В результате оба фактора приводят к снижению растяжимости альвеол.

Доктор Никонов
Мое мнение: у недоношенного ребенка с одной стороны не растягиваются межреберные мышцы, а с другой стороны большая концентрация кислорода сжигает слизистую внутри альвеол. Как только ребенку перестают давать кислород, развивается инфекция в альвеолах в сожженных кислородом местах.
Стадии БЛД
Заключение по результатам патологоанатомических исследований легочной ткани и альвеол у умерших от пневмонии недоношенных детей, которая началась после отстранения ребенка от дыхания кислородом, позволили установить стадии развития БЛД.
Различают 4 стадии формирования диагноза бронхолегочная дисплазия:
- 1 стадия (1-3-й дни жизни новорожденного) – выраженный альвеолярный отек с гиалиновыми мембранами, ателектазами и некрозами эндотелия бронхиол.
- 2 стадия БЛД (4-10-й дни жизни ребенка) – ателектазы становятся более распространенными, чередуются с участками эмфиземы. Некротические массы заполняют воздухоносные пути.
- 3 стадия бронхолегочной дисплазии (11-30-й дни жизни) – распространенная метаплазия и гиперплазия эпителия бронхов и бронхиол, участки эмфиземы, фиброз и отек с истончением базальных мембран альвеол.
- 4 стадия БЛД у недоношенных (второй месяц жизни) – массивный фиброз легких с деструкций альвеол и стенок воздухоносных путей.
В 4 стадии особенно сильно наблюдается гипертрофия мышечного слоя бронхиол, уменьшение количества легочных артериол с гипертрофией мышечного слоя артериол и венул.
Неонатологи лечат недоношенных детей с диагнозом бронхолегочная дисплазия симптоматически: продолжают кислородотерапию.

Доктор Никонов
Мое мнение: неонатологи еще больше сжигают слизистую альвеол. Они применяют бронхолитики, диуретики, глюкокортикостероиды, антиоксиданты и антибиотики.
В острый период при тяжелой степени БЛД, когда стоит вопрос жизни, назначения оправданы. После устранения воспалительного процесса назначение лекарств не решит проблему отека межреберных мышц.
Существует один способ устранения отека из межреберных мышц – воздействие на мышцы по методу Никонова с фиксацией проблемной мышцы.
Последствия и осложнения при бронхолегочной дисплазии
Преимущественное число детей, перенесших на ранних сроках жизни БЛД, страдают нарушениями дыхательной функции в старшем возрасте, при достижении подросткового возраста. Проявлениями нарушений дыхания являются следующие симптомы:
- нарушения проводимости бронхов;
- снижение диффузионной способности;
- гиперинфляция;
- гиперреактивность бронхов.
Все это приводит к следующим заболеваниям:
- рецидивирующий бронхообструктивный синдром (РБОС);
- острые бронхиолиты, особенно связанные с респираторно-синцитиальной вирусной инфекцией;
- хроническая дыхательная недостаточность;
- ателектазы;
- синдром хронической микроаспирации;
- пневмония.
Описанные сочетания бронхолегочной дисплазии с синдромом крупа, врожденными пороками развития легких, трансформация в хронический бронхиолит с облитерацией (ХбсО), бронхиальную астму, рецидивирующий обструктивный бронхит (РОБ).
Новое видео об воздействии на мышцы методом Никонова
Информация на сайте носит ознакомительный характер, собрана из открытых источников. При копировании материалов гиперссылка на klinikanikonova.ru обязательна!
Оставить комментарий
Источник